GASTROENTEROLOGIA - ENDOSCOPIA DIGESTIVA - STUDIO SPECIALISTICO
Menu principale:
- Home Page
- CHI SIAMO
- APPARATO DIGERENTE
-
ENDOSCOPIA DIGESTIVA
- Definizione
- La sedazione
- Disinfezione degli strumenti
- EGDS - GASTROSCOPIA
- ILEO-COLONSCOPIA
- ENTEROSCOPIA
- ERCP
- EUS - ECOENDOSCOPIA
- ENDOSCOPIA OPERATIVA
- GASTRO-DIGIUNO-STOMIE
-
ALTRE METODICHE
- GASTROENTEROLOGICHE
- GASTROFISIOPATOLOGICHE
-
NON GASTROENTEROLOGICHE
- DIAGNOSTICA DI LABORATORIO
- DIAGNOSTICA PER IMMAGINI
- RX CONVENZIONALE
- RX INTERVENTISTICA
-
MALATTIE DELL'INTESTINO
- GASTROENTEROLOGIA - Definizione
- ESOFAGO
- STOMACO
- TENUE
- COLON
- RETTO
- ANO
- VARIE
- MALATTIE DEL FEGATO
- MALATTIE DELLA COLECISTI
- MALATTIE DELLE VIE BILIARI
- MALATTIE DEL PANCREAS
Parassitosi
Parassita: Viene così definito un organismo, vegetale o animale, che vive in un altro organismo di una specie diversa dalla sua.
I parassiti intestinali si dividono in protozoi e metazoi, cioè in organismi unicellulari e pluricellulari.
Come tali, i parassiti protozoi hanno dimensioni particolarmente ridotte (generalmente nell'ordine di pochi μm), mentre i metazoi presentano strutture complesse, differenziamento tissutale e dimensioni decisamente superiori (da pochi mm ad alcuni metri).
I metazoi che interessano la medicina umana, gli elminti (o vermi intestinali), sono distinti in vermi cilindrici (i nematodi) ed in vermi piatti (i platelminti), questi ultimi si dividono ulteriormente in cestodi (di forma nastriforme e segmentata) e trematodi (forma non segmentata).
I parassiti intestinali più comuni:
Protozoi: Giardia lamblia, Dientamoeba fragilis, Entamoeba histolytica, Cryptosporidium sp., Isospora bell e Balantidium coli,
Metazoi: Enterobius vermicularis, Ascaris lumbricoides (ascaridiasi), Trichuris trichiura, Ancylostoma duodenale, Necator americanus, Strongyloides stercoralis, Schistosoma spp. e Taenia spp. [Taenia saginata (dei bovini) e Taenia solium o Erme Solitario (dei maiali)].
Modalità d'infestazione
I parassiti intestinali possono penetrare nell'organismo attraverso l'ingestione di cibi crudi, poco cotti (soprattutto le carni, ma anche pesci) o non adeguatamente lavati (verdure concimate con feci umane o acque nere).
A volte, comunque, anche la stessa acqua diviene un veicolo di trasmissione.
Spesso, soprattutto nel bambino, l'infestazione deriva dall'aver portato ingenuamente alla bocca mani non adeguatamente pulite o aver nuotato in acque contaminate. Altre volte ancora, le larve penetrano direttamente nella cute che prende contatto con il terreno (generalmente le mani od i piedi).
I parassiti intestinali colpiscono elettivamente i bambini (per le minori difese immunitarie e l'attitudine a giocare con il terreno senza poi lavarsi le mani), i soggetti immuno-
Sintomi
Terapia
Il pirantel pamoato è indicato per la terapia della infestazione da ascaridi (ascaridiasi) e della ossiuriasi (infestazione da ossiuro), somministrato in dose unica per via orale, sulla base di 10 mg/kg di peso. Per esempio, un ragazzo del peso di 25 kg dovrà essere trattato con una dose di 250 mg;è sconsigliato nei bambini di età inferiore a 1 anno, in assenza di dati sulla sicurezza d’uso in questa fascia di età.
In pratica, considerati i pesi medi delle varie età pediatriche, la posologia sarà la seguente:
bambini di 1-
bambini di 3-
ragazzi di 6/8 anni: 1 cucchiaino di sospensione o 2 compresse.
Nell'adulto la posologia sarà di 3 compresse fino ad un peso di 85 Kg e di 4 compresse oltre tale peso.
Il mebendazolo è un farmaco antielmintico a largo spettro, attivo sui nematodi e sui cestodi:
• Enterobius vermicularis (ossiuro)
• Ascaris lumbricoides (ascaride)
• Trichuris trichiura (tricocefalo)
• Ancylostoma duodenale (anchilostoma)
• Necator Americanus (anchilostoma)
• Strongyloides stercolaris (strongioloide)
• Taenia spp. (verme solitario)
Una posologia adatta ad ogni indicazione permette di eliminare la totalità dei vermi in più del 90% dei pazienti, anche in caso di infestazioni gravi o miste.
Ossiuriasi: dose unica di 100 mg (una compressa, oppure un misurino da 5 ml di sospensione).
Il ciclo evolutivo dell’Enterobius, agente dell’ossiuriasi, è molto breve. Pertanto i rischi di reinfezione sono molto elevati, specie nelle grandi comunità sociali. Per queste ragioni si consiglia di ripetere il trattamento dopo 2-
Ascaridiasi, tricocefalosi, anchilostomiasi e infestazioni miste: una dose di 100 mg (una compressa oppure un misurino da 5 ml di sospensione) due volte al giorno (mattino e sera), per tre giorni consecutivi, indipendentemente dall’età e dal peso del paziente.
Teniasi e strongiloidiasi
Adulti: benchè si siano ottenuti buoni risultati a dosaggi inferiori, si consiglia una dose di 200-
Bambini: una dose di 100 mg (una compressa oppure un misurino da 5 ml di sospensione) due volte al giorno (mattino e sera), per tre giorni consecutivi.
Le compresse possono essere deglutite con un po’ d’acqua, oppure masticate durante il pasto. Il trattamento non richiede un particolare regime dietetico, né l’uso dei lassativi.
Anisakiasi
L'agente eziologico è l’anisakis, un nematode appartenente alla famiglia Anisakide (generi Anisakis, Pseudoterranova, Hysterothylacium e Contracaecum) che parassita l'intestino di mammiferi marini (delfini, foche ecc.).
Le larve al primo stadio parassitano molte specie di crostacei, mentre le fasi ulteriori si sviluppano in diversi pesci marini tra cui salmoni, aringhe, nasello, merluzzo, che si cibano dei crostacei infestati.
Dopo la pesca, possono migrare nelle carni del pesce a causa di eviscerazione tardiva o marcata infestazione. L'anisakis simplex, l'Anisakis physeteris, o pseudoterranova si possono osservare ad occhio nudo, essendo lunghi a seconda della specie da 1 a 3 cm di colore biancastro o rosato come l'esemplare che è giunto alla nostra osservazione rinvenuto su un filetto di merluzzo fresco acquistato al supermercato. L'uomo è un ospite occasionale di questo parassita che si contagia consumando pesce crudo o affumicato parassitato dalle larve che, una volta ingerite, vengono generalmente neutralizzate dall’apparato digerente, oppure possono penetrare nella parete dello stomaco e dell’intestino dove muoiono successivamente.
Patogenesi
Il parassita provoca a livello locale una reazione infiltrativo -
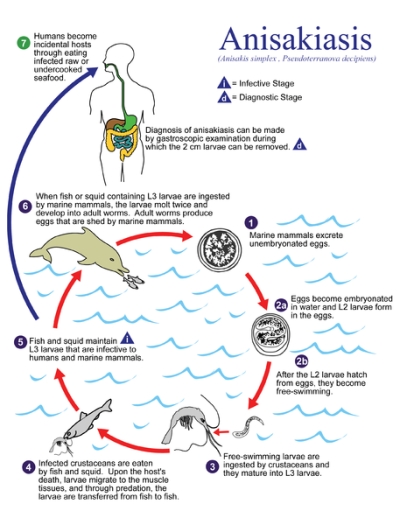
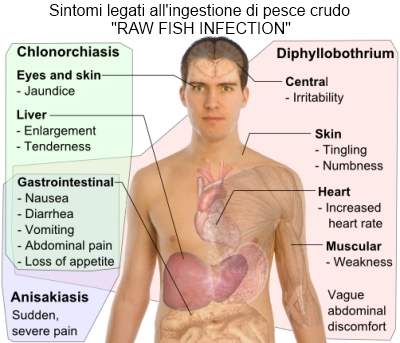
Tale constatazione potrebbe essere associata all’assunzione di preparazioni alimentari in precedenza considerate sicure. Reazioni di ipersensibilità IgE-
Sintomatologia
Dolori addominali, nausea sono i sintomi che più frequentemente si associano alla malattia. Possono essere presenti fenomeni occlusivi o perforazioni determinate dalla formazioni granulomatose. In altri rari casi, oltre all’interessamento del tratto gastroenterico, vi può essere l’invasione di altri organi come i polmoni, il fegato, la milza, il pancreas ecc. Quadri clinici di allergia possono essere messi in relazione al parassita.
Diagnosi
Ci si avvale dell’esame istologico eseguito mediante indagine endoscopica (EGDS) e per via chirurgica, non essendo disponibile un test diagnostico di laboratorio.
Terapia e profilassi
Al momento non si dispone di farmaci sicuramente efficaci. La terapia è sintomatica e basata sulla rimozione del parassita per via endoscopica o chirurgica. La prevenzione costituisce la migliore terapia. Il parassita è molto resistente agli acidi, ma non alla cottura e al congelamento (-
Verme solitario
La tenia (Taenia) è un verme piatto parassita, di aspetto nastriforme, in grado di vivere anche nell’intestino umano; i vermi comunemente identificati come tenia (od anche verme solitario) sono in realtà appartenenti a diverse specie:
Taenia crassiceps
Taenia pisiformis
Taenia saginata
Taenia solium (VERME SOLITARIO, presente nella carne suina)
I parassiti adulti sono vermi nastriformi, piatti, segmentati ed ermafroditi appartenenti alla famiglia dei platelminti. La loro lunghezza varia generalmente dai 5 ai 10 metri e sono costituiti dallo scolice, dal collo e da segmenti non maturi, in fase di maturazione e maturi in successione lineare.
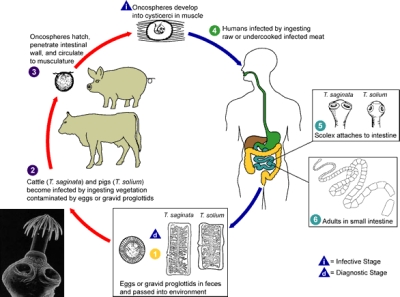
Le proprietà che caratterizzano il parassita adulto dal punto di vista morfologico e fisiologico rispecchiano il fatto che, da un lato, la tenia è straordinariamente specializzata per sopravvivere nell’intestino dei vertebrati e, dall’altro lato, ha considerevoli capacità riproduttive, rese possibili dalle unità sessuali multiple, i segmenti o proglottidi. La specie riesce così a far fronte all’enorme tasso di perdita di segmenti o uova che vengono espulsi con le feci, e dalla probabilità piuttosto remota che l’uovo riesca a raggiungere l’ospite intermedio e quindi si trasferisca all’interno di un altro essere umano.
La parte terminale del parassita (una frazione variabile dalla metà a un terzo) è costituita da segmenti in fase riproduttiva, che al loro interno ospitano le uova: sono fatti di tessuto muscolare e si muovono esattamente come i millepiedi, quindi possono raggiungere lo sfintere anale ed essere espulsi nell’ambiente. In questo modo sono in grado di infettare gli ospiti intermedi erbivori.
La ciste larvale della tenia, detta cisticerco, è una ciste a contenuto liquido, delle dimensioni di un pisello, che si insedia nei muscoli dell’ospite intermedio. All’interno della ciste c’è un scolice invertito, formato da una porzione germinativa della parete interna della cisti.
Infestazione
Se un essere umano mangia carne bovina/suina infetta cruda o non ben cotta, il cisticerco viene digerito, si apre e inverte lo scolice, che si attacca alle pareti dell’intestino tenue e inizia a produrre la lunga catena di segmenti. Dopo circa tre mesi il parassita avrà già raggiunto i 4, 5 metri di lunghezza e i segmenti in fase riproduttiva inizieranno a essere espulsi. Il verme è estremamente longevo: può sopravvivere anche per 5, 20 anni o più.
Sintomi
Si limitano a: episodi di nausea o vomito, diminuzione dell’appetito, dolore epigastrico o ombelicale, diarrea, stitichezza, dimagrimento.
È anche possibile rilevare un’eosinofilia (quantità di eosinofili nel sangue) moderata. Una manifestazione piuttosto allarmante e imbarazzante della presenza della tenia è la fuoriuscita dei segmenti del parassita in grado di muoversi dall’ano. In rari casi può verificarsi anche la perforazione intestinale.
Trasmissione
La tenia, il più frequente dei parassiti platelminti dell’essere umano, viene trasmesso sottoforma di cisticerchi ai bovini: è possibile vedere che il bovino è infetto perché la sua carne presenta piccole macchie caratteristiche. La carne bovina non ben cotta, affumicata od in salamoia può essere infetta, ma il meccanismo di trasmissione più frequente dell’infezione è la carne cruda (carne alla zingara o tritata), come testimonia la frequenza della teniasi nei paesi come l’Etiopia e l’Argentina, dove la carne cruda o non ben cotta è un alimento molto comune.
Terapia
La niclosamide è un farmaco non assorbito dall’intestino umano che, entrando in contatto con lo scolice e i segmenti anteriori del verme solitario, li uccide, provocando l’espulsione del parassita.
Adulti e bambini oltre 6 anni: 4 compresse; bambini da 2 a 6 anni: 2 compresse; bambini al di sotto di 2 anni: 1 compressa.
Nelle infezioni da Hymenolepis nana (tenia nana) si consiglia un trattamento di 7 giorni. Primo giorno: adulti e bambini oltre 6 anni, 4 compresse; bambini da 2 a 6 anni, 2 compresse; bambini al di sotto di 2 anni, 1 compressa. In ognuno dei successivi giorni: adulti e bambini oltre 6 anni, 2 compresse; bambini da 2 a 6 anni, 1 compressa; bambini al di sotto di 2 anni, mezza compressa. L'intera dose giornaliera va assunta subito dopo la colazione del mattino; le compresse vanno masticate fino ad essere ridotte ad un impasto omogeneo che va deglutito con poca acqua. Possono anche venire disciolte in un liquido e poi ingerite. Nei bambini piu' piccoli vanno opportunamente ridotte ad un impasto omogeneo prima di essere somministrate con poco liquido.
Il praziquantel, un derivato di sintesi dell’isochinolina-
Questi ed altri medicinali vengono impiegati spesso in associazione a lassativi, per favorire la naturale eliminazione del parassita e delle uova. Qualora tali farmaci non fossero sufficienti si può ricorrere ad un piccolo intervento chirurgico.
Prevenzione
Il controllo della carne per evidenziare la presenza dei cisticerchi è la miglior misura preventiva possibile. Nelle aree endemiche la carne deve essere sempre consumata ben cotta e deve raggiungere una temperatura di almeno 56 °C in tutte le sue parti. Può essere difficile realizzare una cottura del genere nel caso di tagli grandi di carne grassa, in particolare di maiale. Il congelamento a -
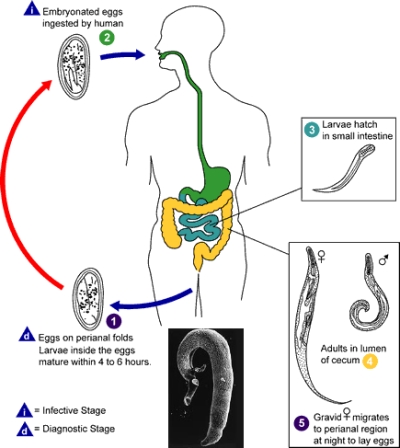
Ossiuriasi
L'Enterobius vermicularis, conosciuto anche come "verme dei bambini" o ossiuro, è un parassita bianco e sottile, responsabile di una patologia nota come ossiuriasi. Oltre al cane, colpisce anche la specie umana e si manifesta elettivamente nei bambini, in modo particolare in quelli che vivono in ambienti affollati, in comunità scolastiche numerose o in condizioni di scarsa igiene. La femmina adulta dell'Ossiuro è lunga approssimativamente un centimetro con una sezione pari a circa 0,5 mm, mentre il maschio è più piccolo (2-
Infestazione
L'ossiuriasi viene contratta per ingestione delle uova embrionate, che possono arrivare alla bocca attraverso il cibo o tramite contatto diretto di mani ed oggetti contaminati. Dopo l'ingestione le larve si schiudono nel primo tratto dell'intestino tenue e si sviluppano nelle porzioni ad esso contigue. Mano a mano che si trasformano in vermi adulti, gli ossiuri discendono il tubo digerente fino a raggiunge l'intestino crasso (cieco, appendice e colon discendente), dove vivono per circa 7-
Dopo la fecondazione, i maschi vanno rapidamente incontro a lisi, mentre le femmine disaderiscono dalla mucosa e migrano di notte verso l'apertura anale, dove depongono circa 10.000 uova, per poi morire in meno di mezz'ora. Al contrario di quanto avviene per molti altri parassiti, le uova degli ossiuri diventano infestanti già dopo pochi minuti dalla loro deposizione. Per questo motivo le infestazioni da uomo a uomo sono frequenti, così come il fenomeno dell'autoinfestazione. Gli ossiuri possono essere facilmente trasmessi anche da bambini ad adulti.
Sintomi
L'infestazione da ossiuri è relativamente innocua e riconosce nel prurito perianale il suo sintomo più comune. Questo segno, che si fa più intenso e molesto nelle prime ore notturne, spinge la persona a grattarsi e a raccogliere involontariamente le uova, che verranno poi disperse con le mani nell'ambiente circostante. Il prurito da ossiuri si estende frequentemente anche nell'area vaginale e perineale (spazio compreso tra ano e genitali); talvolta è talmente fastidioso da disturbare il sonno e causare cefalea, irrequietezza ed evidenti lesioni da grattamento.
Altri sintomi di interesse clinico sono il dolore addominale e vari problemi di natura gastrointestinale (nausea, vomito ecc.). Raramente, in seguito alla migrazione del parassita, si possono verificare fenomeni di appendicite acuta o di salpingite cronica (processo infiammatorio di una o di entrambe le tube di Falloppio).
Diagnosi
Oltre che al reperto visivo degli ossiuri nelle feci e nella zona perineale (da effettuarsi preferibilmente nelle ore notturne o al risveglio), la diagnosi di ossiuriasi si basa su un semplice esame, chiamato "scotch test", che consiste nell'appoggiare una sottile striscia di carta adesiva sull'apertura anale del paziente. Anche questa operazione andrà eseguita al mattino, prima dell'evacuazione e del successivo lavaggio. Le uova del parassita rimaste adese alla parte collosa dello scotch verranno poi facilmente identificate all'esame microscopico.
Terapia
Gli ossiuri sono particolarmente sensibili al trattamento con diversi farmaci, come il pirantel pomoato (che provoca un blocco neuro-
Giardiasi
è una malattia dell’apparato digerente causata da un parassita microscopico (un protozoo) di nome Giardia lamblia.
Il parassita si attacca alla parete interna dell’intestino tenue del paziente dove interferisce con il normale assorbimento dei grassi e dei carboidrati, che avviene durante la digestione.
La Giardia Lamblia è una delle principali cause di diarrea negli Stati Uniti e si trasmette attraverso l’acqua contaminata; può sopravvivere anche alla normale quantità di cloro usata per purificare le scorte d’acqua potabile e resistere per più di due mesi in acqua fredda. Bastano soltanto 10 minuscoli parassiti in un bicchier d’acqua per causare una forma grave di giardiasi in un essere umano che li beve.
I bambini sono tre volte più a rischio degli adulti per quanto concerne la giardiasi e proprio per questo alcuni esperti ritengono che il nostro organismo sviluppi gradualmente una qualche forma di immunità al parassita con l’andare dell’età. E’ comunque abbastanza frequente che un’intera famiglia si ammali di giardiasi: alcuni membri della famiglia possono avere la diarrea, altri soltanto dolori addominali crampiformi ed altri ancora pochi sintomi o addirittura nessuno.
Sintomi
Si stima che in alcuni Paesi occidentali una percentuale variabile dall’uno al venti per cento della popolazione sia affetta da giardiasi e la percentuale può aumentare oltre il 20% nei paesi in via di sviluppo, dove la giardiasi è una delle principali cause delle epidemie di diarrea tra i bambini.
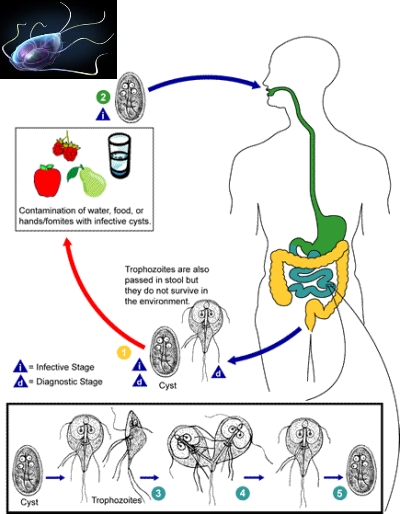
Più dei due terzi delle persone infette, tuttavia, possono non presentare segni né sintomi della malattia, anche se il parassita si è insediato nel loro intestino. Se il parassita provoca dei sintomi la malattia di solito inizia con forti episodi di diarrea, che al suo interno non contiene né sangue né muco. La giardia impedisce l’assorbimento dei grassi alimentari da parte del nostro organismo, quindi le feci espulse contengono i grassi che non sono stati assorbiti con il risultato che gli escrementi galleggiano, si presentano lucide ed emanano un pessimo odore.
Tra gli altri sintomi troviamo: crampi addominali, consistente produzione di gas intestinali, gonfiore dovuto ai gas, diminuzione dell’appetito, nausea e vomito, in alcuni casi, febbre di lieve intensità.
Questi sintomi possono durare per 5-
A volte, passati i sintomi acuti (o a breve termine) della giardiasi, la malattia si cronicizza ed entra in una fase più prolungata con sintomi diversi: formazione ricorrente di gas intestinali, dolore addominale nella zona sopra l’ombelico, feci molli e non strutturate.
Diagnosi
La diagnosi è resa possibile dall'evidenziazione nelle feci dei caratteristici trofozoiti o delle cisti. Questi sono facilmente rinvenuti nelle infezioni acute, ma l'eliminazione del parassita è intermittente e a bassi livelli nella infezione cronica. La diagnosi può richiedere perciò ripetuti esami delle feci o l'esame del contenuto dell'intestino superiore ottenuto con una striscia di nylon o per aspirazione endoscopica. Per l'evidenziazione dei parassiti o dei loro antigeni sono disponibili test di immunofluorescenza ed ELISA.
Terapia
Il metronidazolo orale (250 mg tid per 5 giorni negli adulti; 15 mg/kg/die in tre dosi frazionate per 5 giorni nei bambini) è efficace. Gli effetti collaterali includono nausea, cefalea e, meno comunemente, urine scure, parestesia e vertigini. Il furazolidone orale (100 mg qid per 7-
I familiari o i partner sessuali del paziente vanno esaminati e curati se colpiti dalla giardiasi. La terapia durante la gravidanza deve essere evitata; se possibile, il metronidazolo non deve essere somministrato a donne in gravidanza. Se la terapia non può essere ritardata a causa di sintomi gravi, può essere usato un aminoglicoside non assorbibile come la paromomicina (25-
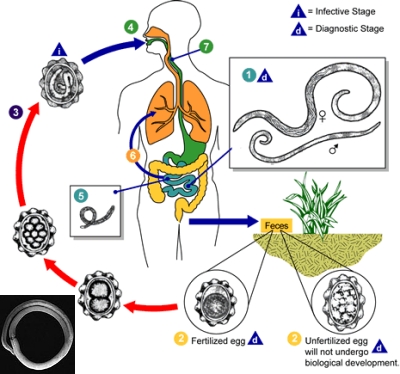
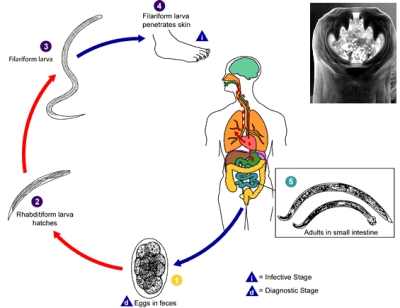
Ascaridiasi
Gli ascaridi sono i responsabili di un’infezione intestinale, l’ascaridiasi, ancora abbastanza comune fra i bambini; gli ascaridi sono vermi tondi, parassiti dell’intestino di uomini ed animali. Pur essendo la più comune infezione umana causata da vermi in tutto il mondo, gli ascaridi sono tuttavia sempre meno frequenti nella popolazione del mondo occidentale; si verifica infatti in prevalenza nelle altre zone del mondo, con frequenza più ampia nelle zone di scarsa igiene o dove le condizioni di vita sono affollate e promiscue.
L’ascaridiasi si verifica più spesso nei paesi in via di sviluppo, dove le condizioni igienico sanitarie sono scarse, o in zone in cui le feci umane sono ancora usate come fertilizzanti.Il verme dell’ascaridiasi (Ascaris lumbricoides) attecchisce quando le uova del parassita vengono ingerite: le uova possono essere assunte da alimenti o acqua contaminata, dal suolo o da feci di soggetti infetti.
Quando le uova vengono ingerite arrivano all’intestino dove, schiudendosi, diventano larve; una volta oltreppasata la parete intestinale le larve viaggiano dal fegato fino ai polmoni attraverso il flusso sanguigno.
Durante questa fase possono comparire dei sintomi polmonari come la tosse, anche tosse con vermi. Dai polmoni le larve risalgono attraverso i bronchi fino alla gola, dove sono nuovamente inghiottite. Facendo ritorno al piccolo intestino crescono, maturano, si accoppiano e depongono uova, raggiungendo la maturità circa due mesi dopo che l’uovo originario è stato ingerito dal suolo. I vermi adulti vivono e rimangono nel piccolo intestino, possono crescere e diventare spessi come una matita, lunghi da cm 15 a cm 40 (quaranta!) ed in grado di vivere da uno a due anni.
Un verme femmina può produrre fino a 240.000 uova in un giorno, che sono poi scaricate nelle feci ed incubate nel suolo per settimane. I bambini sono particolarmente esposti a rischio di ascaridiasi perché tendono a mettere le cose in bocca, compresa immondizia, e spesso hanno abitudini igeniche più scarse degli adulti.
Sintomi
Anche se possono non verificarsi sintomi, più vermi sono coinvolti nell’infestazione, più gravi saranno i sintomi che bambini e adulti potranno manifestare. I bambini hanno più probabilità rispetto agli adulti di sviluppare sintomi gastrointestinali perché i loro intestini sono più piccoli ed hanno maggiori rischi di sviluppare ostruzioni intestinali.
I sintomi osservati dalle manifestazioni più lievi includono: vermi nelle feci, tosse con vermi, perdita di appetito, febbre, respiro affannoso.
Infestazioni più gravi possono portare ad un quadro più severo, con: vomito, mancanza di respiro, distensione addominale (gonfiore del ventre), dolore allo stomaco o all’addome, ostruzione intestinale, ostruzione delle vie biliari (inclusi fegato e cistifellea).
Trasmissione
L’ascaridiasi non si diffonde direttamente da una persona all’altra. Per essere infettati gli individui hanno bisogno di consumare le uova del verme.
Terapia
Di solito prescrive i farmaci antiparassitari (Mebendazolo, Pirantel Pamoato) da assumere per via orale per uccidere i nematodi intestinali. A volte le feci vengono riesaminate circa tre settimane dopo il trattamento per verificare la presenza di uova e di vermi. I sintomi di solito scompaiono nel giro di una settimana dall’inizio del trattamento. Molto raramente può essere necessaria la rimozione chirurgica del verme (in particolare nei casi di ostruzioni intestinali, del fegato o di infezioni addominali). Un bambino che ha l’ascaridiasi dovrebbe essere controllato per altri parassiti intestinali, come i vermi comuni.
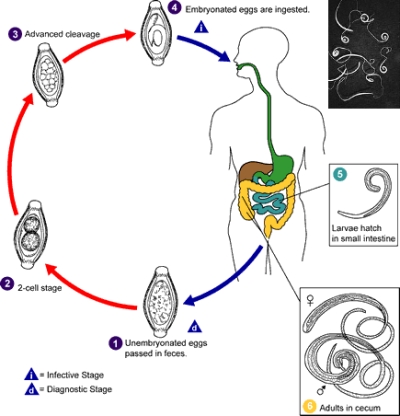
Trichiuriasi
(o Infezione da vermi a frusta o Tricocefalosi) indica l'infezione da Trichuris trichiura, che causa dolore addominale e diarrea.
Eziologia e patogenesi
L'infezione si diffonde per via oro-
Sintomi, segni e diagnosi
Le infestazioni lievi sono spesso asintomatiche, mentre quelle più gravi causano dolore addominale, anoressia e diarrea e possono ritardare l'accrescimento. Le infestazioni massicce possono causare perdita di peso, anemia e prolasso rettale nei bambini e nelle partorienti. Nelle feci vengono facilmente rinvenute le caratteristiche uova a forma di limone.
Prevenzione e terapia
La prevenzione richiede un'adeguata igiene ambientale e personale. Non è necessario alcun trattamento per le infestazioni asintomatiche o lievi. Il mebendazolo (100 mg PO bid per 3 giorni) viene usato per le infestazioni più gravi. Il farmaco non deve essere usato durante la gravidanza.
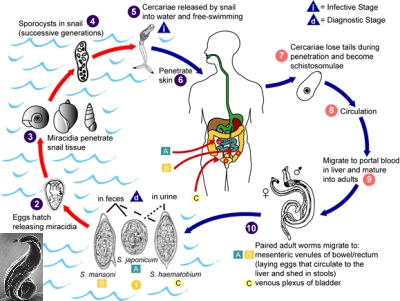
Schistosomìasi
(o bilharziosi o distomatosi sanguigna), malattia parassitaria causata da vermi del genere Schistosoma. Schistosoma mansoni e Schistosoma japonicum risiedono nelle venule dell'intestino e danno origine a manifestazioni epatiche; entrambi i parassiti sono presenti solo nelle zone tropicali dell'America Meridionale, dell'Africa e dell'Asia. Schistosoma haematobium si localizza nelle venule del tratto urinario e determina infestazione vescicale. Il contagio avviene mediante il contatto con acque inquinate dal parassita (allo stadio di cercaria), il quale penetra attraverso la cute e nell'organismo si trasforma in schistosomula. Dopo due o tre giorni migra nel circolo venoso, depone le uova e dà origine a vermi che rimangono nel circolo venoso. I soggetti infetti eliminano con le feci e le urine le uova, che vengono captate da molluschi d'acqua dolce o terrestri (ospiti intermedi) e danno origine alle cercarie.
Nei paesi dove è endemica, la schistosomìasi è spesso asintomatica, oppure si manifesta con sintomi gastrointestinali, epatici, polmonari e vescicali. In alcune zone (per esempio, Egitto) l'infezione vescicale è strettamente correlata con il carcinoma della vescica. La terapia va riservata a casi con specifica indicazione, poiché è gravata di effetti collaterali e non distrugge il parassita, ma inibisce soltanto la produzione delle uova. Il farmaco più usato a tale scopo è il praziquantel.
Anchilostomiasi
o infezione da anchilostoma, è un'infezione intestinale causata dall'Ancylostoma duodenale o Necator americanus. La diagnosi clinica è difficile dato che l'infezione non produce sintomi specifici. L'identificazione delle uova dell'anchilostoma nelle feci durante l'esame microscopico è indicativa dell'infezione. Si stima che gli anchilostomi infettino oltre 1.300 milioni di individui nel mondo. L'infezione è una causa importante di emorragia intestinale, che produce anemia da deficit di ferro (IDA). L'anchilostomiasi colpisce una parte significativa della popolazione nelle aree tropicali e subtropicali, in quanto le condizioni igieniche e climatiche sono particolarmente favorevoli alla sua trasmissione. Nei Paesi sviluppati l'infezione da anchilostoma è rara, però può essere osservata tra i viaggiatori che rientrano da Paesi in via di sviluppo o tra gli immigrati. Sono indicati quattro farmaci per il trattamento delle infezioni da anchilostoma (albendazole, levamisole, mebendazole, pyrantel pamoato). Nelle aree endemiche la strategia raccomandata per il controllo della malattia è il trattamento periodico (una o due volte all'anno). Lo stesso approccio è suggerito per cittadini che appartengono a Paesi sviluppati e che vivono temporaneamente nelle aree endemiche.